共价键
分析:Cl2和HCl分子的形成的过程。
氯原子的结构示意图和电子式:
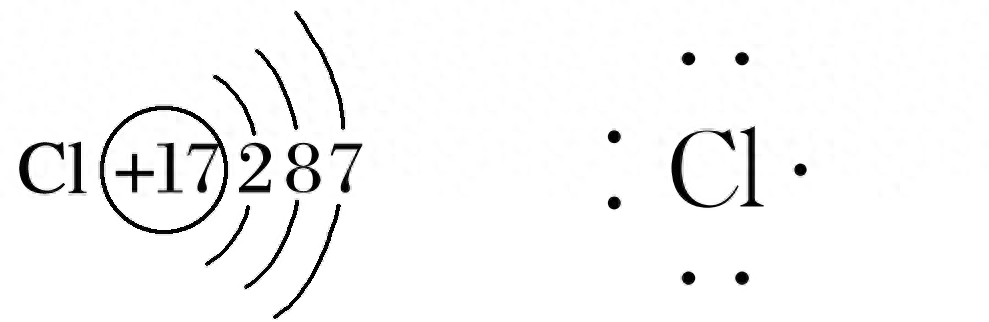
氯气的形成过程:两个氯原子都想得1个电子成为8个电子的稳定结构,所以两个氯原子只能各拿1个电子,形成共用电子对,同时围绕两个原子核运动,这样两个氯原子均达到8个电子的稳定结构,双方通过共用电子对产生静电作用,形成稳定的氯气分子。
用电子式表示其形成过程:
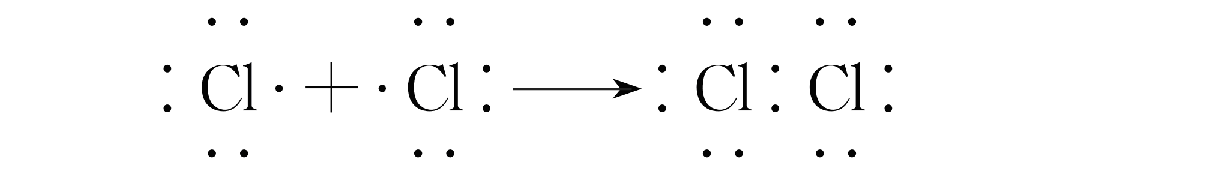
HCl的形成过程:氢原子和氯原子都想得1个电子成为2个和8个电子的稳定结构,所以双方各提供一个电子,形成共用电子对,同时围绕两个原子核运动,双方都达到稳定结构。
用电子式表示其形成过程:
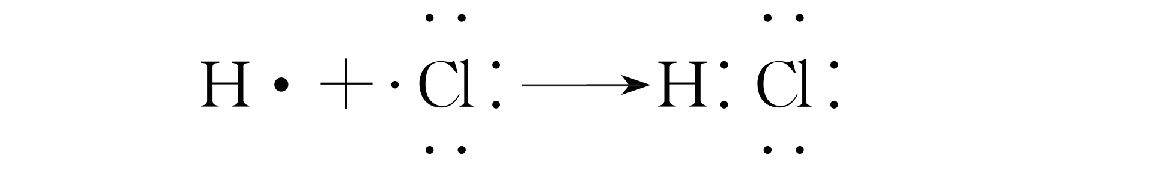
这种通过形成共用电子对产生的强烈的相互作用,叫共价键。本质上仍然是一种静电作用。
象HCl这种通过共用电子对形成的化合物叫共价化合物。常见的共价化合物有酸、非金属氧化物、非金属氢化物、大部分的有机物,还有一些盐,如AlCl3也是共价化合物。
共价化合物一般由原子通过共价键形成分子,分子组成化合物。也有一些共价化合物由原子直接构成,不存在分子,如SiO2。
Cl2由同种元素的原子形成共价键,成键的双方吸引电子的能力相同,共用电子对不偏移,成键原子不显电性,这样的共价键属于非极性共价键,简称为非极性键。
HCl由不同种元素的原子形成共价键,氯原子吸引电子的能力更强,共用电子对偏向Cl一方,带少量负电荷,共用电子对偏离H一方,带少量正电荷,这样的共价键属于极性共价键,简称非极性键。
共价键小结:
原子间通过共用电子对所形成的强烈的相互作用。

共价键小结
共价化合物是通过共用电子对形成分子的化合物。

共价化合物的分类
可用电子式表示共价键、共价化合物及其形成。也可以用结构式表示,用一个短横代表一个共用电子对即单键,用双横代表双键,用三横代表三键。
如,Cl2的电子式、结构式:
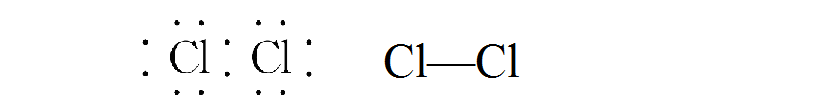
N2的电子式、结构式:

还可以用分子结构模型表示。

视频加载中...
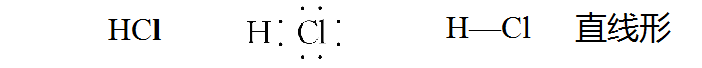
视频加载中...
视频加载中...
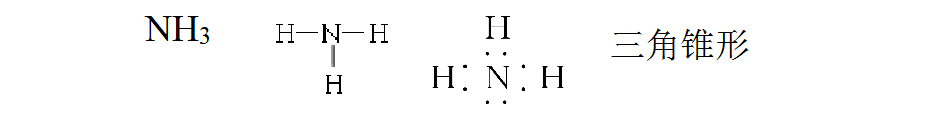
视频加载中...
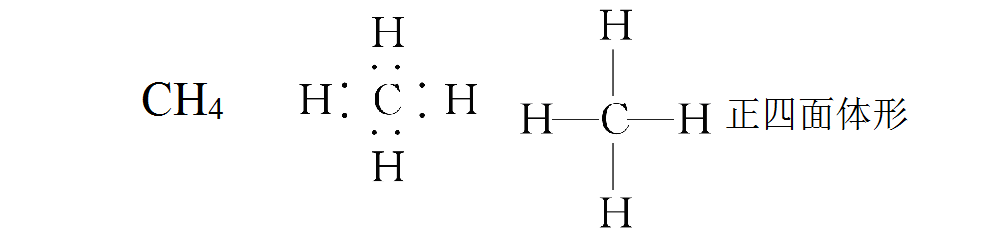
视频加载中...
视频加载中...
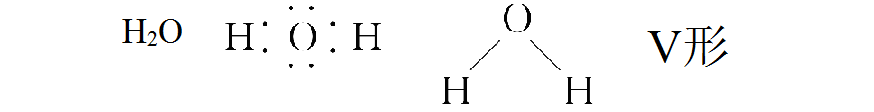
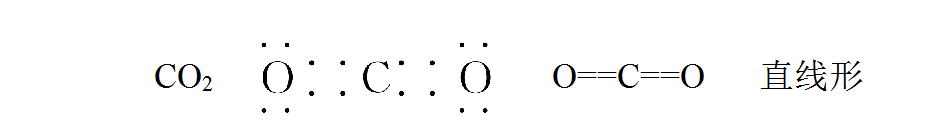
几种常见的电子式和结构式:
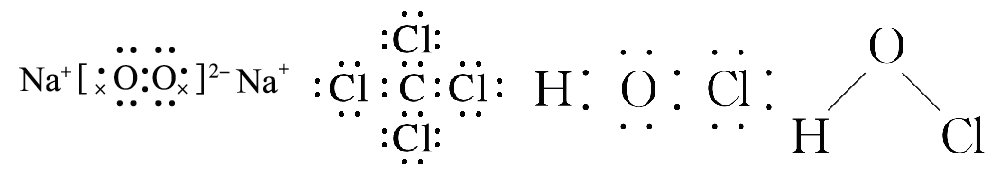
化学反应的本质:
从宏观角度分析,化学变化是生成了新物质;从微观的角度看,化学变化是原子的重新组合。以H2和Cl2反应为例,分析化学变化中原子在重新组合时,化学键发生了什么变化。
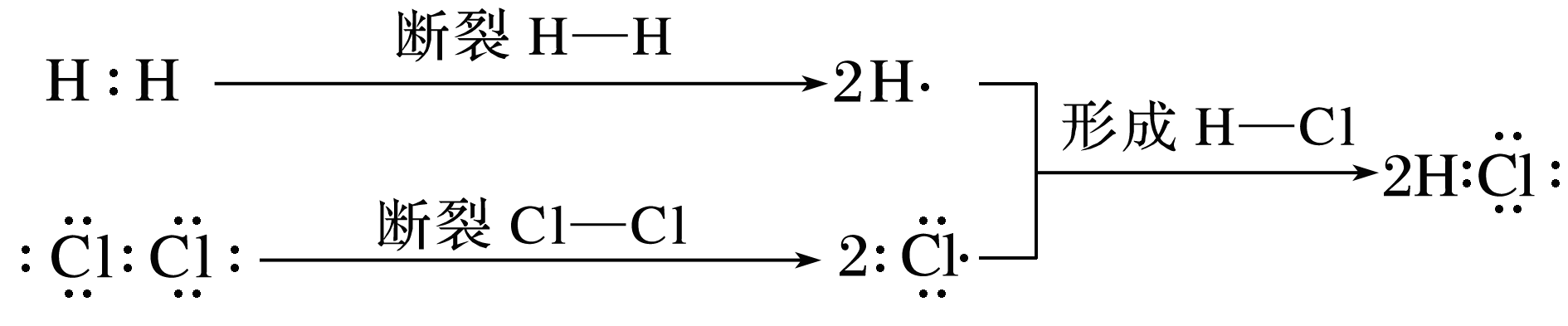
氢气分子中的H-H键断裂成为H原子,氯气分子中的Cl-Cl键断裂成为Cl原子,然后一个H原子和一个氯原子形成H-Cl。
可见化学变化的本质是旧化学键的断裂和新化学键的形成。
化学键知识小结:
化学键是相邻的原子之间强烈的相互作用。
化学键的分类。
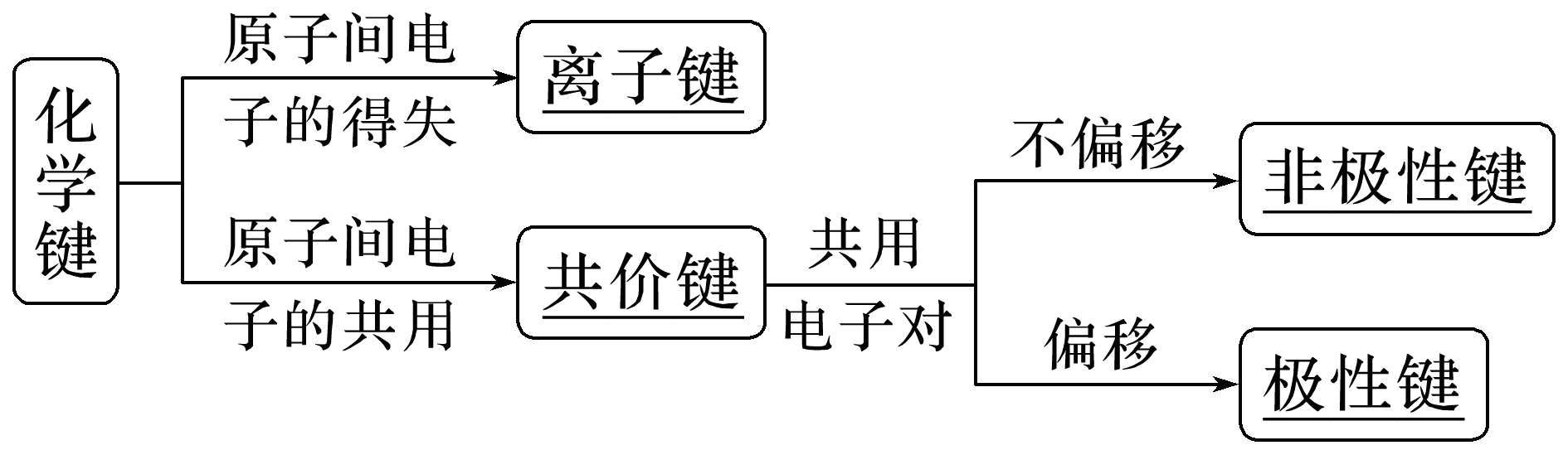
化学键的分类
两种化学键的比较。
离子键 | 共价键 | |
概念 | 带相反电荷的离子之间的相互作用 | 原子之间通过共用电子对所形成的相互作用 |
成键方式 | 通过得失电子达到稳定结构 | 通过形成共用电子对达到稳定结构 |
成键粒子 | 阴、阳离子 | 原子 |
形成条件 | 活泼金属元素与活泼非金属元素化合(非金属元素也可形成) | 同种或不同种非金属元素(也可以有金属元素和非金属元素)结合 |
存在 | 离子化合物中 | 绝大多数非金属单质、共价化合物、某些离子化合物中(有原子团的) |
分子间作用力:
由分子构成的物质在状态发生变化时,会有热量的放出和吸收,说明分子间存在一种把分子聚集在一起的作用力,叫分子间作用力,最初又称范德华力。由分子构成的物质,其熔、沸点等物理性质主要由分子间作用力大小决定。
分子间作用力分为范德华力和氢键。其中范德华力比化学键弱得多;氢键不是化学键,比化学键弱,比范德华力强。
分子间形成的氢键会使物质的熔点和沸点升高。如,水分子间的氢键可使其形成缔合分子(H2O)n,熔点、沸点相对偏高,水结冰时会产生空隙,密度变小,体积膨胀。有些物质在水中的溶解性也与氢键有关。
思考:
1、除了化学变化外,还有哪些过程中化学键会破坏。
离子化合物都是电解质,在溶解或熔化时会电离,离子键被破坏得到阴、阳离子。
共价化合物中的电解质(酸)在溶解或熔化时情况不同,溶解时发生电离,共价键被破坏生成阴、阳离子,在熔化时破坏分子间作用力,共价键不断裂。非电解质,如蔗糖、酒精溶解和熔化时共价键不被破坏,还有一些会破坏共价键。

单质的熔化或溶解过程:
①由分子构成的固体单质,如碘I2的升华、白磷P4的熔化只破坏分子间作用力,而不破坏化学键。稀有气体没有化学键,就不存在化学键的断裂。
②由原子构成的单质,如金刚石、晶体硅,熔化时破坏共价键。
③对于某些活泼的非金属单质,溶于水后,能与水反应,其分子内共价键被破坏,如Cl2、F2等。
2、下列反应过程中,同时有离子键、极性共价键和非极性共价键断裂和形成的反应是。
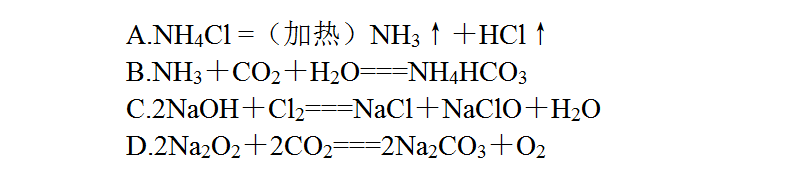
反应物和生成物中都必须含有离子键、极性键和非极性键。NH4Cl中不含非极性共价键,NH3、CO2、H2O 中都不含离子键和非极性键, NaCl、NaClO、H2O中都不含非极性键,Na2O2中含有离子键、非极性键,CO2中含有极性键,Na2CO3中含有离子键、极性键,O2中含有非极性键,D项正确。
